| 所属 |
① 東京大学 大学院薬学系研究科 ② 北里大学 薬学部 |
|
|---|---|---|
| 氏名 |
① 楠原 洋之 ② 前田 和哉 |
|
| AMED 事業 |
課題名 | 新規薬効成分の薬物動態解析と体内動態特性予測の支援 |
| 代表機関 | 東京大学 | |
| 代表者 | 楠原 洋之 | |
in vivo薬物動態、実験動物、体内動態、薬物速度論解析
一般に、薬物が効果を適切に発現するためには、薬効発現に関連した標的となる組織に薬物が到達することがまず必要である。さらに、薬物の標的組織中濃度が薬効発現において十分な薬物濃度に到達し、かつ適切な時間、標的組織に滞留し、一定時間後に消失することが最適な薬効のために必須である。本支援テーマでは、薬効評価モデル動物における薬物暴露の確保を目指した一連の研究手技および動態解析を支援する。具体的には、実験動物へ薬物を投与後、経時的な採血を行うことで、血中濃度の時間推移を得ると共に、適宜、組織の採材を行い、血中・組織中薬物濃度の定量を行う。血液中では、血球への薬物の分配やアルブミン等の血中タンパク質への薬物の結合があるが、薬効に関連するのは、血中に蛋白非結合形として存在している薬物濃度(遊離形濃度)である。臨床で用いられる濃度範囲においては、薬物の血中遊離形濃度は、総濃度と比例関係にあるケースがほとんどであり、その係数をin vitro実験にて測定することで、薬効発現に必要な投与量を推定することができる。そのための実験(平衡透析・限外ろ過等)も支援可能である。また、静脈内投与であれば、投与した薬物量が100%血液中に到達するが、経口投与の場合、消化管での溶解/吸収、肝初回通過効果等が余分に存在するため、薬物によっては、期待したほど循環血中に到達しないことも生じ得る。低暴露の要因を明らかにするため必要な実験方法の提案(in vitro/in vivo)、実験データの速度論解析の支援も行う。シーズ化合物の薬効標的組織への分布も考慮し、有効性・安全性評価に繋がる体内動態研究をトータルに支援する。また、静注・経口以外の投与経路となる薬物の解析についても、研究者の希望にできるだけ対応したいと考えている。
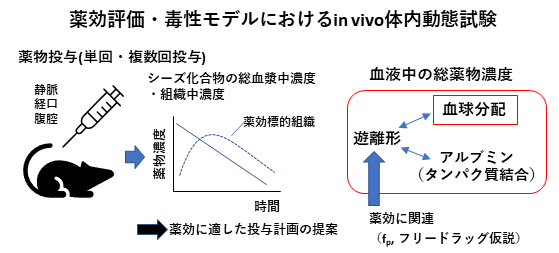
シーズ化合物に対して、実験動物における有効性評価を行うにあたり、薬物を単回・繰り返し投与し、血中薬物濃度の推移や滞留性(消失半減期)を評価する。In vitro/in silico試験の結果、十分な薬効が期待される推定濃度との比較により、実験動物で効果が得られる投与量を推定する。
脳など局所の組織内での作用発現を期待するシーズ化合物については、血液中に加えて、組織中の薬物濃度を測定し、薬効標的組織に薬物が十分量移行しているか、薬物濃度が標的タンパク質との相互作用の速度論パラメータを考慮した際に十分な値を達成しているかを検証し、十分な薬効発現を達成するために必要な投与量を推定する。また、シーズ化合物が、経口投与されても十分に薬効発現しうる薬物濃度が達成できるかについて、経口投与し、血中濃度を測定する。期待したほどの濃度が得られない際には、静脈内投与試験を対照とし、マスバランスを考慮することで低暴露の要因を推定し、シーズ化合物の構造展開の際のパラメータの目標値を設定すると共に、シーズ化合物の体内動態特性を改善するための実験方法の提案を行う。
楠原と前田は、①体内動態に関連する分子、主にトランスポーターによる組織分布・排泄の重要性を解明することを目的として、胆汁排泄や尿排泄など実験動物におけるin vivo薬物動態試験、②in vivoデータをサポートするため、肝臓などの初代培養細胞や薬物トランスポーターの強制発現系などin vitroモデルの開発、③ヒトにおける薬物動態や医薬品を複数服用した際の体内動態の変動(薬物相互作用)を予測するため、in vitroデータの外挿方法(in vitro-in vivo extrapolation/in vitro-in vivo correlation)を開発してきた。薬物速度論に基づいて、薬物固有の動態特性を表すパラメータを決定することで、体内動態におけるトランスポーター分子の重要性を定量的に評価してきた。特に研究②では、実験動物に加えて、ヒト由来試料として、ヒト肝細胞(遊離あるいは接着型)を用いた薬物輸送試験、代謝試験の実績を有する。さらに最近、腸管クリプト由来幹細胞を拡大培養し、その後分化させることで、小腸における薬物吸収・代謝をin vitroで評価する試験系を確立し、in vitroモデルにおける薬物動態関連分子の重要性を評価する実験系を確立している。幹細胞を拡大培養し得られるスフェロイドや、分化誘導後の小腸吸収上皮細胞を含むスフェロイドを調製し、薬物動態・毒性試験における有用性の実証へ向けた研究を展開している。腸管クリプト由来幹細胞については、実験動物に加えて、ヒト由来細胞の構築にも取り組んでいる。In vitro試験系で評価した薬物動態パラメータを数多く収集すると共に、生体における組織重量や血流速度等生理学的なパラメータも考慮した薬物動態の数理モデルを構築し、個体レベルへの薬物動態特性の外挿法、既存薬物のin vitroデータと臨床データを参照し、その相関関係に基づいて予測性を改善する方法(研究③)も開発してきた。また、薬物動態研究として、健常人を対照とした臨床研究(特定臨床研究)により、in vitro試験の予測結果を検証することにも取り組んでいる。
研究室HP:https://dotai.f.u-tokyo.ac.jp/ja/index.html